Physiologie de l’hémostase
L’hémostase regroupe l’ensemble des phénomènes naturels qui permettent l’arrêt du saignement en cas de blessure, de choc ou d’intervention chirurgicale. L’arrêt du saignement, aussi appelé coagulation, se produit suite à la formation d’un caillot qui vient obturer la brèche (ou colmater la blessure) qui s’est formée au niveau d’un vaisseau. La formation de ce caillot fait intervenir plusieurs acteurs qui vont entrer en scène à des moments différents. On distingue classiquement trois périodes interdépendantes: tout d’abord l’hémostase primaire puis l’étape de la coagulation plasmatique qui permettent l’arrêt du saignement. La troisième étape, la fibrinolyse, permet de dissoudre le caillot une fois qu’il a rempli son rôle et de restaurer l’intégrité du vaisseau.
L’hémostase primaire
Figure 1 : Représentation de l’hémostase primaire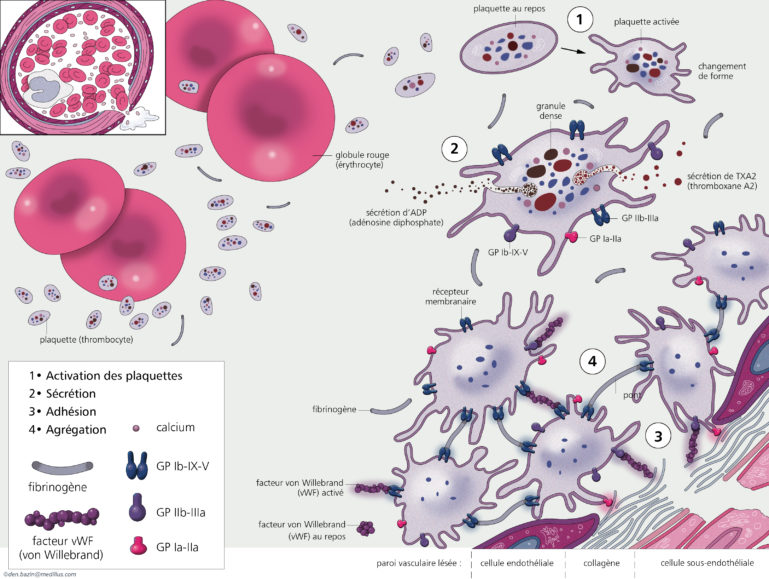
Les principaux acteurs de l’hémostase primaire sont les vaisseaux, les plaquettes et deux facteurs : le fibrinogène et le facteur von Willebrand (VWF), qui participent également à la coagulation.
Parmi les molécules d’adhésion qui jouent un rôle important sur la plaquette il faut citer les glycoprotéines (GP) GPIb-IX-V qui se lient au facteur Willebrand présent au niveau du sous endothélium et la GPIa-IIa qui se fixe au collagène également présent au niveau du vaisseau lésé. Le facteur Willebrand se lie également au collagène du sous endothélium. Lorsque les plaquettes adhèrent au sous-endothélium par l’intermédiaire du VWF, la GP IIb-IIIa peut alors fixer le fibrinogène qui forme des ponts entre les plaquettes activées (agrégation). Le VWF peut également former un pont entre deux molécules de GP IIb-IIIa. En dehors de ces molécules d’adhésion présentent à la surface des plaquettes, des petits granules présents à l’intérieur de ces cellules vont également jouer un rôle important. En effet, lorsque les plaquettes adhérent au vaisseau lésé elles sont activées et libèrent dans la circulation le contenu de leurs granules ce qui va favoriser et entretenir leur agrégation. Des réactions biochimiques ont également lieu à l’intérieur des plaquettes activées, elles permettent la formation de molécules qui favorisent et stabilisent l’agrégation des plaquettes et donc le clou plaquettaire formé. Ces réactions permettent également aux plaquettes activées d’exposer à leur surface des phospholipides (PL) qui vont participer à la phase suivante : la coagulation.
La coagulation plasmatique
Figure 2 : Schéma de la cascade de la coagulation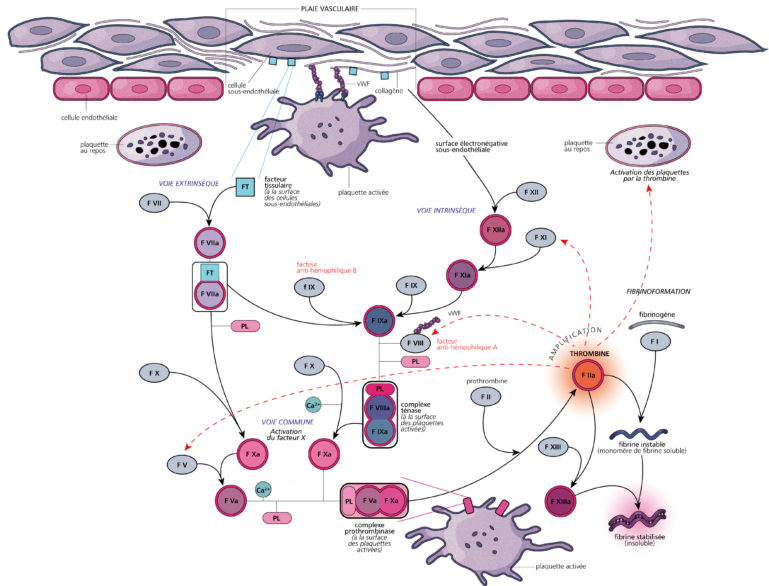
Lorsque le clou plaquettaire est formé sa structure doit être consolidée par les mailles d’un filet formé par la fibrine. Cette fibrine se forme lors de la coagulation plasmatique et provient de la transformation du fibrinogène en fibrine (Figure 2). On observe rapidement une gélification du sang due à la transformation du fibrinogène soluble en fibrine insoluble. Cette transformation est la conséquence de l’action d’une enzyme : la thrombine. La thrombine (FIIa) ne peut circuler dans le sang sous sa forme enzymatique et existe donc sous une forme inactive la prothrombine (FII). Son activation résulte d’une série d’activation d’autres molécules enzymatiques (facteurs de la coagulation) qui elles aussi circulent dans le sang sous forme inactive. On parle de cascade de la coagulation.
Le déclenchement de la coagulation a lieu lorsque le sang circulant rentre en contact avec du facteur tissulaire (FT). Ce FT n’existe pas en circulation mais est présent au niveau du sous endothélium mis en contact avec le sang par la brèche vasculaire. Le FT se fixe au facteur VII (FVII) de la coagulation qui est activé en FVIIa. Le complexe FT/FVIIa va, en présence de phospholipides (PL) et de calcium, former un complexe enzymatique qui active un autre facteur circulant, le facteur X en facteur X activé (FXa). Ces phospholipides proviennent des cellules vasculaires lésées et des plaquettes activées. A son tour, le facteur Xa se regroupe avec le facteur V sur les PL pour former le complexe prothrombinase qui active la prothrombine en thrombine toujours en présence de calcium. La thrombine va alors transformer le fibrinogène soluble en fibrine insoluble.
Le complexe FT/Facteur VII activé est également capable d’activer le facteur IX ou facteur anti‑hémophilique B. Le Facteur IXa se fixe à la surface des PL en présence de facteur VIII (facteur anti‑hémophilique A) pour former un complexe enzymatique activateur du FX qui rejoint la voie de la coagulation initiée par le FT. Dans la circulation le facteur von Willebrand transporte le FVIII et le protège de la dégradation enzymatique.
Le Facteur X peut également être activé par d’autres voies d’activation. Lorsque le sang est au contact d’une surface électronégative (telle que le verre), la coagulation se déclenchera sans faire appel au FT. Cette surface est capable d’activer le facteur XII qui lui-même activera le facteur XI et ce dernier activera le Facteur IX. Le facteur IX activé en présence de facteur VIII de PL et de calcium pourra activer le Facteur X en Facteur Xa.
La formation de la thrombine (thrombinoformation) est un phénomène explosif, la thrombine est capable d’amplifier la cascade de la coagulation et donc sa propre formation. De plus la thrombine active les plaquettes et favorise l’étape de l’hémostase primaire.
Inhibition de la coagulation
Tout système d’activation, comme celui de la coagulation, possède un système naturel inhibiteur afin d’éviter son emballement. L’inhibition de la coagulation a lieu principalement grâce à 4 inhibiteurs. L’antithrombine qui comme son nom l’indique inhibe la thrombine mais également la plupart des facteurs activés (enzymes) de la coagulation. Le couple de la protéine C et de la protéine S qui inhibent les facteurs VIII et V de la coagulation et enfin le TFPI (inhibiteur de la voie du FT) qui inhibe le facteur VIIa couplé au facteur tissulaire.
Fibrinolyse : dissolution du caillot de fibrine
Lorsque de la fibrine s’est formée dans l’organisme celle-ci devra être dissoute lorsque le saignement s’est arrêté. Cette phase est appelée fibrinolyse. De nouvelles enzymes interviennent comme la plasmine qui va couper la molécule de fibrine et la rendre soluble. Cette étape contribue également à la réparation du vaisseau blessé.
Vidéo de la physiologie de la coagulation +
Jeu « COAGULATION INTERVENTION BRIGADE »
Le jeu de réalité virtuelle pour les patients atteints de déficits en facteur de coagulation appelée « Coagulation Intervention Brigade (CIB) » disponible sur Youtube complète l’explication de la physiologie de la coagulation.
Ce jeu CIB est une application mobile en réalité virtuelle développée par le Pr Négrier du CRTH de Lyon et le Laboratoire Français de Biotechnologie des Biomédicaments (le LFB Biomédicaments) et il est destiné aux patients atteints de déficits en facteurs de coagulation. L’internaute muni de lunettes spécifiques permettant la vision en 3D peut jouer avec les différentes protéines de la cascade de la coagulation en ayant la perception de se situer eu cœur du vaisseau sanguin.
Liens:
AppStore: https://goo.gl/K7ZjMh
Google Play: https://goo.gl/CSVEvH






